زیست شناسی
این وبلاگ برای تمام عزیزانی که به علوم زیستی علاقه دارند ایجاد شده و از همه چیز و همه جا که مرتبط با زیست شناسی باشد اطلاعات میدهد
زیست شناسی
این وبلاگ برای تمام عزیزانی که به علوم زیستی علاقه دارند ایجاد شده و از همه چیز و همه جا که مرتبط با زیست شناسی باشد اطلاعات میدهدآیا می دانید
اختلالات ناخن
1- لکههای سفید رنگ: علت آن میتواند صدمه به ماتریکس و یا کمبود روی ‹++Zn باشد اما زیاد مهم نبوده و به مرور زمان ناپدید میگردد.
2- عفونتها: میتواند عامل آن باکتریها و یا قارچها باشند که در هر دو صورت باید به پزشک مراجعه شود.
3- شیارهای روی ناخن: این شیارها اغلب ارثی میباشند اما اگر یکباره روی ناخنها آشکار گردند علت آن میتواند ضربه، پیری، روماتیسم و یا بیماری کلیه باشد.
4- حفره روی ناخن: علت آن میتواند اگزما و یا ضربه باشد.
5- قاشقی شکل شدن ناخن: علت آن کمکاری تیروئید(هیپوتیروئیدسیم)، کنبود آهن و کمخونی میباشد.
6- شکاف در لبه ناخن: علت آن فرو بردن انگشتان به مدت زیاد در آب داغ، اختلال در جریان خون، کمبود ویتامینهای و B6 و نیاسین، کمبود آهن و کلسیم و کمکاری تیروئید باشد. کمآبی بدن بسیار مهم است بنابراین آب فراوان بنوشید.
7- ناخنهای فرو رفته در گوشت: این شکل بیشتر در ناخنهای پا مشاهده میگردند و علت آن کوتاه کردن نامناسب ناخنها و کفش تنگ میباشد که باعث میگردد گوشه ناخن به درون گوشت فرو رود.
8- برخی بیماریها از روی ناخن
ناخن قرمز نشانه بیماری قلبی- ناخنهای سفید رنگ نشانه بیماری کبدی- ناخن ضخمی و زرد رنگ نشانه بیماری ریوی- سرخی مختصر در ته ناخن نشانه دیابت و ناخنهای دو رنگ نیمی سفید و نیمی صورتی نشانه بیماری کلیه میباشد.
تهیه و تنظیم: بابک صدیقی
سمینار در رابطه با گیاه بومادران
با سلام
مطلب زیر سمیناری است در رابطه با خواص دارویی گیاه بومادران که توسط اینجانب تهیه و ارایه شده است . لازم به ذکر است به دلیل طولانی بودن مطلب فقط مقدمه و چکیده آورده شده است.
مقدمه
امروزه با پیشرفت علم به خصوص در زمینه ی ساخت مواد و لوازم بهداشتی و دارویی مشاهده می شود توجه همگان بر روی موادی است که به استانداردهای جهانی نزدیکتر باشد ثانیا عوارض جنبی آن نیز کم باشد لذا ناخواسته مصرف کننده با توجه به پیشینه ی قبلی و سنتی که در ذهن خود دارد تمایل زیادی به استفاده از داروهای گیاهی را دارد به همین منظور شرکتهایی را مشاهده می کنیم که رو به سوی ساخت انواع داروهای گیاهی آورده اند و از طرف دیگر مشاهده میشود این امر با اقبال عمومی نیز همراه است.
یکی از مسایل مهم امروز که مورد توجه است بهداشت فردی است. بهداشت فردی به معنی مراقبت از جسم و روان فرد برای حفظ تندرستی و پیشگیری بیماری است در حقیقت فرد سالم به کسی گفته میشود که نه تنها از سلامت جسم و روان برخوردار باشد بلکه از نظر اجتماعی نیز در رفاه و آسایش باشد. بنابراین بهداشت فردی شامل مراقبت و نظافت از پوست – مو – چشم – گوش – دهان – دندان و دستگاههای مختلف بدن می باشد که نگهداری هر کدام از آنها برای سلامت انسان لازم و ضروری است.
همانطور که می دانیم پوست یکی از اعضای مهم و وسیع بدن است. پوست اولین پوشش بدن در برابر عوامل بیماریزا است زیرا خارجی ترین قسمت آن از سلولهایی تشکیل شده که از عبور میکروبها به بافت زیر پوست جلوگیری می کند و در مقابل میدانیم که برای درمان آسیبی که به پوست وارد میشود ، اگر از برخی داروهای شیمیایی استفاده شود نه تنها بطور کامل باعث ترمیم بافت آسیب دیده نمیشود بلکه ممکن است اثرات جانبی نیز بر جای بگذارد به همین دلیل امروزه افراد ترجیح میدهند از داروهای گیاهی ، حتی با وجود اینکه دوره ی درمانی طولانی تری نسبت به داروههای شیمیایی دارند اما موثرتر و نسبتا بی زیان تر از مواد شیمیایی هستند استفاده کنند.
لذا ما در این طرح با توجه به نیاز جامعه بر آن شدیم که یکی از داروهای سنتی را که در درمان ترک پا موثر است را بصورت علمی اثبات و بکارگیری نماییم.
چکیده
بررسی ها و تحقیقات علمی نشان داده که داروهای گیاهی در مقایسه با سایر داروهای شیمیایی از عوارض جانبی بسیار کم و یا هیچ برخوردار است لذا امروزه در درمان بسیاری از بیماریها سعی بر این است که بسیاری از این گیاهان را جایگزین داروهای شیمیایی کنند .
در این طرح پژوهشی نیز یکی از همین گروه از گیاهان سنتی به نام بومادران(Achillea micruntha) که دارای خواص دارویی بسیار از جمله: کاهنده قند خون – بند آورنده خونروی از بینی – رفع اختلالات بینایی و ... اشاره کرد را مورد بررسی قرار دادیم. گیاه بومادران به دلیل خود رو بودن و اینکه به آسانی در بیشتر نقاط ایران یافت میشود هزینه ی زیادی را برای تهیه و جمع آوری در بر نمیگیرد، لذا می تواند از نظر اقتصادی تا حد زیادی به صرفه باشد و با توجه به اینکه این گیاه دارای موادی است که میتواند پوست را چرب نگه بر آن شدیم تاثیرات این گیاه را بر روی ترک پا مورد آزمایش علمی قرار دهیم.
گیاه مورد نظر را از مزرعه زیست شناسی دانشگاه اراک تهیه کرده و پس از جدا کردن گلها و تمیز کردن ، آنها را در مجاورت هوای آزاد خشک کردیم سپس در هاون کوبانده و به روش پرکولاسیون عصاره ی گیاه را استخراج نمودیم و پس از تعیین گروههای نمونه و شاهد مراحل تجویز عصاره انجام گرفت که با بررس کیفی و آماری نتایج زیر به دست آمد:
بعد از تجویز عصاره به بیماران مورد نظر و با توجه به جدول زمان بندی، زمان بهبودی ترک پای آنها به این ترتیب بود: ترک پای 21 نفر بعد از چهارده روز بهبودی کامل یافت و 13 نفر بعد از پانزده روز و 3 نفر بعد از شانزده روز و 5 نفر بعد از سیزده روز ، 2 نفر بعد از دوازده روز ، 3 نفر بعد از یازده روز و 3 نفر باقیمانده پس از ده روز ترک پایشان بهبودی کامل حاصل کرد که پس از بهبودی نیز هیچگونه عوارض جانبی از طرف این عصاره مشاهده نگردید لذا میتوان نتیجه گرفت گیاه بومادران در بهبود و درمان ترک پا موثر بوده و میتواند جایگزین مناسبی برای داروهای شیمیایی باشد.
تحقیق از: بابک صدیقی - دبیر و دانشجوی ارشد زیست شناسی
ریبوزم
ریبوزم
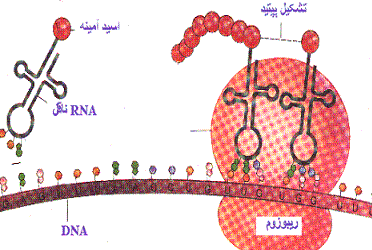
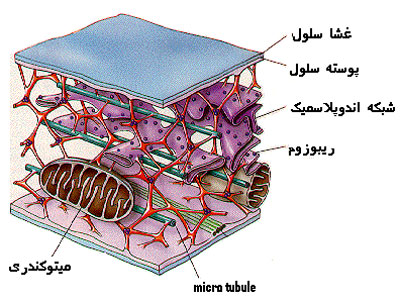
ریبوزمها از اندامک های بدون غشای سیتوپلاسمی در همه یاختههای پروکاریوتی و یوکاریوتی هستند که در سال 1983 بهوسیله پالاد کشف شدهاند. این اندامک ها را دانههای پالاد نیز مینامند. از آنجا که سنتز پروتئین ها بهوسیله ریبوزوم ها صورت میگیرد اهمیت زیادی دارند. ریبوزوم ها ذراتی کم و بیش کروی، متراکم (کدر) نسبت به الکترون ها هستند که نظرشان از 40 تا حدود 300 آنگستروم میرسد.
تاریخچه شناخت ریبوزومها
شناخت اولیه ریبوزوم ها مربوط به کلود میشود که در سال 1941 با مرکزگریزی شدید (اولتراسانتریفوگاسیون) افتراقی (مرحلهای) موفق به جداسازی ذراتی کوچکتر و سبکتر از میتوکندری ها شد که ذراتی به قطر 500 تا 2000 میکرون و سرشار از RNA بودند که از خرد شدن قطعات شبکه آندوپلاسمی ضمن اولترا سانتریفوگاسیون ایجاد میشوند. میتوانند حتی در شرایط آزمایشگاهی اسیدهای آمینه پرتوزا را به سرعت در ساختمان پروتئین ها وارد کنند.
اشکال ریبوزومها
ریبوزم های آزاد سیتوپلاسمی که در سیتوپلاسم یاختههای پروکاریوتی از نوع 70s در سیتوپلاسم یاختههای یوکاریوتی از نوع 80s یعنی بزرگتر و سنگینتر هستند.
ریبوزوم های چسبنده به غشای شبکه آندوپلاسمی دانهدار که این حالت تنها در یاختههای یوکاریوتی که شبکه آندوپلاسمی دارند، دیده میشود. در این یاختهها نسبت ریبوزمهای آزاد سیتوپلاسمی به ریبوزمهای چسبیده به غشای شبکه بر حسب شرایط فیزیولوژیکی یاخته تغییر میکند و هر چه سنتز پروتئینهای ترشحی و پروتئینهای ساختمانی ویژهای که در ساختمان غشای شبکه آندوپلاسمی، غشای کیسههای گلژی، لیزوزومها و پلاسمالم وجود دارند بیشتر باشد، نسبت ریبوزومهای چسبیده به غشای شبکه نیز بیشتر میشود.
در یاختههای ترشحی آسینیهای باز لوزوالمعده که آنزیمهای گوارشی مختلف را میسازند و یاختههای خونی که ایمنوگلوبینها را میسازند تا 90% ریبوزومها به غشای شبکه آندوپلاسمی چسبیدهاند. بر عکس در رتیکولوسیتها، بافتهای مریستمی گیاهان و یاختههای عصبی رویانی بیشتر ریبوزومها آزادند. در یاختههای هلا که نوعی یاخته سرطانی هستند تنها 15% ریبوزومها به غشای شبکه چسبیدهاند.
ریبوزومهای موجود در اندامکهای مثل ریبوزومهای میتوکندری و ریبوزومهای کلروپلاستی: این ریبوزومها نیز تنها در یاختههای یوکاریوتی وجود دارند. ضریب ته نشینی آنها بر حسب گونه یاختهها متفاوت است و به هر حال سبکتر و کوچکتر از ریبوزومهای سیتوپلاسمی یاخته مربوط هستند. از نظر ساخت و کار، حساسیت به آنتی بیوتیکها و بیش از آن ابعادشان به ریبوزومهای پروکایوتی شبیهاند.
نحوه قرارگیری ریبوزوم ها
ریبوزومهای سیتوپلاسمی، اندامکی و ریبوزمها چسبنده به غشای آندوپلاسمی میتوانند به حالت منفرد (مونوزوم) یا به حالت چند تایی (پلی زوم) باشند. مجموع حدود 5 تا 80 ریبوزوم را که به مولکولی از mRNA چسبیدهاند، پلی زوم نامند. ریبوزومها تنها وقتی که به حالت پلی زوم باشند، سنتز پروتئین دارند. گاهی در سیتوپلاسم پلی زومها حالت مارپیچی یا حلزونی به خود میگیرند فراوانی این نوع پلی زومها در یاخته را نشانه نوعی اختلال در فرآیند سنتز پروتئین میداند.
تعداد ریبوزوم ها در یک یاخته
تعداد ریبوزمهای یک یاخته تا حدود پانصد هزار میرسد. این تعداد در یاختههای مختلف و نیز در شرایط مختلف زیستی و فیزیولوژیکی در یک یاخته تغییرات زیادی دارد. در یک یاخته باسیل کولی حدود ده هزار تا پانزده هزار ریبوزوم موجود است. در اغلب در پروکاریوتها حدود 104، در یوکاریوتها حدود 105 تا 107 و در اووسیتها بطور معمول بیش از 1012 ریبوزوم وجود دارد.
عمر متوسط ریبوزوم ها
عمر متوسط ریبوزومها در حدود 6 ساعت است. بنابراین بازسازی پیوسته آنها ضرورت دارد. سرعت بازسازی در یاختههای مختلف 10 تا 100 ریبوزوم در هر ثانیه است. بازسازی ریبوزومها در یاختههای پروکاریوتی در سیتوپلاسم و بیتردید ضمن رونویسی از ژنهای rRNA و در یاختههای یوکاریوتی در ارتباط با هستک صورت میگیرد ترکیبات بازدارنده رونویسی و همچنین سم آمانیتین که در قارچ آمانتیا وجود دارد این بازسازی را متوقف میکنند.
روشهای جداسازی و مشاهده ریبوزوم ها
به روشهای مختلف زیر میتوان ریبوزومها را جداسازی و مشاهده کرد ساکارز و حضور Mg+2 جدا میکنند. اولترا سانتریفوگاسیون به مدت یک ساعت و 100000gr انجام میشود. برای جدا کردن ریبوزومها از غشای شبکه آندوپلاسمی از دزوکسی کولات سدیم یا بکارگیری محلولهای نمکی دارای غلظت مناسب و انجام اولترا سانتریفوگاسیون استفاده میشود.
تمام مراحل جداسازی باید با حضور غلظت مناسبی از یونهای Mg+2 صورت گیرد. این غلظت مناسب با استفاده از کلرور منیزیم 0.01 مولکول گرم در لیتر تامین میشود. در غلظتهای زیاد آن (بیش از 0.1 مولکول گرم در لیتر) ریبوزومها به هم میچسبند و به حالت دیمر در میآیند و در غلظت 0.001 مولکول گرم در لیتر کلرور منیزیم دو جزء ریبوزوم از هم جدا میشوند.
ریختشناسی ریبوزوم ها
از دو بخش کوچک و بزرگ تشکیل یافته است. در باسیل کولی، بخش کوچک کشیده، خمیره و دارای قسمتی متراکم و پیچیده است. بخش کوچک در گودی سطح فوقانی بخش بزرگ قرار گرفته است. بخش کوچک در 3/1 طول خود دارای دندانهای کوچک است و مقابل به دانه دارای قسمتی متراکم و پیچیده است. بخش کوچک در گودی سطح فوقانی بخش بزرگ قرار گرفته است و حدود 3/1 از حجم کل ریبوزوم را تشکیل میدهد. بخش بزرگ که 3/2 حجم کل ریبوزوم را شامل میشود دارای یک سطح گود (مقعه) و سه زایده است.
سطح مقعر جایگاه چسبیدن بخش کوچک ریبوزومی است. زواید بخش بزرگ انگشت مانند، کوتاه و در انتها مدورند. زایده میانی بزرگتر و زواید جانبی کوچکترند. بخش بزرگ ریبوزوم از نیم رخ حالتی شبیه صندلی را حتی با یک بخش پشتی و در جای دست دارد. در یوکاریوتها بخش بزرگ شبیه آن باسیل کولی است اما یک زایده طویل است که به سوی سمت راست بخش بزرگ کشیده شده است.
پروتئین سازی نقش اصلی ریبوزوم ها
پروتئینها از ماکرومولکولهای اساسی یاختههای هستند که بیش از نیمی از وزن خشک آنها را میسازند. در ساختار اندامکها و اجزای فعال یاختهها یافت میشوند و در ساخت و کار آنها نقش بنیادی دارند. ماکرومولکهای پروتئینی از ترکیب اسیدهای آمینه با اتصالهای کووالانسی پپتیدی ایجاد میشوند. در بیوسنتز آنها از جمله ریبوزومها، RNA های پیامبر، RNA های ناقل و ... شرکت دارند. وقتی که ریبوزومها در سنتز پروتئینها فعال نیستند اغلب به صورت ذخیرهای از اجزای آزاد در سیتوپلاسم پراکندهاند.
منبع:دانشنامه رشد.
بیماری آأکاپتونوریا
بیماری آلکاپتونوریا
۱-الکاپتونوریا:یک بیماری متابولیکی ارثی است که در اثر نقص انزیم اسیدهموژنتیسیک اکسیداز در مسیر متابولیکی فنیل الانین-تیروزین ایجاد می شود.این بیماری اختلال اتوزومی مغلوب اتوزومال رسسیو است.فقدان انزیم هموژنتیسیک اسید اکسیداز متابولیسم فنیل الانین-تیروزین را درمرحله اسید هموژنتیسیک مهارمی سازد.بنابراین اسیدهموژنتیسیک دربدن تجمع می یابد.به طورطبیعی
اسیدهموژنتیسیک درخون یا ادراروجودندارد
ولی درالکاپتونوریا این اسید دربین سلولها و داخل سلولهابه صورت گراندلریاهوموژن تجمع می یابدومقادیرزیادی ازآن ازطریق ادراردفع میگردد.اکسیداسیون و پلی مریزاسیون این ترکیب درادرار(کهنه)ودرمعرض هوا قرارگرفته ماده ای شببه ملانین وسیاه رنگ را به وجود می آورد که تیرگی ادرارنظیر جوهر(urine as ink)را سبب می گردد.
2- اوکرونروز چیست؟
َاسید هموژنتیسیک علاوه بر رسوب مستقیم دربافتها با مهار آنزیم لیزیل ئیدروکسیلاز مهارکننده بیوسنتز کلاژن نیز هست بدین ترتیب که اسیدهموژنتیسیک نگهداری شده دربدن به طورانتخابی به الیاف کلاژن بافت همبند و تاندونها و وترعضلانی وغضروفها متصل شده وآنها را به رنگ آبی مایل به سیاه در می آورد.اوکرونروز اصطلاحی است که تیره شدن بافتهارا توصیف می کند
به دلیل تجمع پلیمر سیاه اسیدهموژنتیسیک در غضروف و بافتهای مزانشیمی دیگر میباشد.اوکرونروز در بافتهای مختلف مانند غضروفها(بینی.گوش.دنده.حنجره.نای.مفاصل)و تاندونها و نسوج نرم(گونه.دست.فقرات....)اپیدرم.اندوکارد و انتیمای عروق.کلیه.پروستات.ریه.صلبیه.ملتحمه و قرنیه.پرده صماخ رخ می دهد ولی بیشتر در گوشها.بینی و گونه ها دیده می شود .
و به دلیل تجمع پلیمر سیاه اسیدهموژنتیسیک در غضروف و بافتهای مزانشیمی دیگر میباشد.اوکرونروز در بافتهای مختلف مانند غضروفها(بینی.گوش.دنده.حنجره.نای.مفاصل)و تاندونها و نسوج نرم(گونه.دست.فقرات....)اپیدرم.اندوکارد و انتیمای عروق.کلیه.پروستات.ریه.صلبیه.ملتحمه و قرنیه.پرده صماخ رخ می دهد ولی بیشتر در گوشها.بینی و گونه ها دیده می شود .
3- چگونه الکاپتونوریا بر مفاصل تاثیر می گذارد ؟
جدی ترین عارضه اوکرونروز ناشی از رسوب رنگدانه ها درغضروفهای مفصلی می باشد.به دلایل نامشخصی این پیگمانتاسیون موجب می شود که غضروف لغزندگی طبیعی خود را از دست داده شکننده و شیاردار گردد.فرسایش و پاره شدگی این غضروف رشته رشته به درون استخوان زیرین رانده می شود و باعث تشدید بیشتر آسیب می گردد.ستون مهره ای و مخصوصا دیسک بین مهره ای اولین هدف این تهاجم است.اما بعدا مفاصل زانوها شانه ها و لگن ممکن است مبتلا شوند.مفاصل کوچک دستها و پاها معمولا مبتلا نمی شوند با آنکه نقص متابولیکی از هنگام تولد وجود دارد.آسیب مفصلی دژنراتیو به آهستگی به پیش می رود و معمولا با دهه چهارم زندگی از نظر بالینی قابل تشخیص نمی باشد .
آرتریت در مردان معمولا شدیدتر است.آرتریت ناشی از این بیماری خصوصیات بالینی آرتریت روماتیسمی را دارد ولی در پرتونگاری خصوصیت استئوآرتریت را دارا می باشد.تغییرات دژنراتیو و مهره های کمری همراه با کم شدن فضای مفصلی و چسبیدن جسم مهره ها مشخصه بیماری است پاتوژنز تغییرات آرتریتی هنوز مشخص نشده است . آسیب مفصلی دژنراتیو با وجود آنکه تهدیدی جهت ادامه زندگی نیست ناتوانی موجود در اشکال حاد استئوآرتریت افراد مسن می باشد ولی در عارضه آلکاپتونوری این آرنروپاتی در سنین بسیار پایینی رخ می دهد.
نظرات تکمیلی
بیماری " آلکاپتونوریا " نوعی بیماری ژنتیکی است که در اثر نارسایی در فرایند تجزیهی اسیدآمینههای فنیل آلانین و تیروزین به وجود میآید. این بیماری پیامد کمبود آ نزیمی است که اسید هموجنتیسیک (آلکاپتون) را به اسید مالیل استواستیک تبدیل میکند. در اثر کمبود این آنزیم، که هموجنتیسیک اسید اکسیداز نام دارد، آلکاپتون در بدن بیمار انباشته میشود و از راه ادرار به بیرون راه مییابد . این نارسایی به بیماری خطرناکی نمیانجامد، اما وقتی ادرار در برخورد با هوا قرار میگیرد، آلکاپتون با اکسیژن واکنش میدهد که پیامد آن، تبدیل آلکاپتون به فراوردهای تیره رنگ است و این فراورده باعث تیره شدن رنگ ادرار میشود. از این رو، مردم عادی نوزادنی را که با این نارسایی به دنیا میآمدند، انسانهایی سیاه بخت و تیره روز میپنداشتند.
آرچیبلد گرود با پژوهش گستردهای که روی این بیماری انجام داد، به این نتیجه رسید که این نارسایی، به علت یک عامل ژنی نادر (باتوار ث مندلی) رخ میدهد و ازدواج بستگان درجهی اول، زمینهی بروز این صفت نهفته و نادر را آماده میسازد. برای این پژوهش بود که نظریهی " یک ژن، یک آنزیم " ، با نام این پژوهشگر گره خورد. البته، همانطور که در ادامه میخوانید، وی با گردآوری و تفسیر دادههای به دست آمده از پژوهشهای دانشمندان دیگری، به این مفهوم پایهای دست پیدا کرد.
در پژوهشهای گرود، کمتر با طراحی آزمایش روبهرو میشویم. در حقیقت ، او با مشاهده و گردآوری اطلاعات توانست، فرضیههای خود را تا اندازهای اثبات کند. سرانجام، زیستشیمیدانها با پژوهش هایی که طی نیم سده انجام دادند، توانستند تصویر دقیقتری از اساس بیماری آلکاپتونوریا عرضه کنند.
در این مقاله، شما با شیوهی پژوهشی گرود آشنا میشوید و درمییابید که چگوه گردآوری دادهها و تفسیر آنها به یک یافتهی زیستشناسی میانجامد.
طرح مسئله
در سال 1898 میلادی، خانوادهای به دکتر گرود مراجعه کردند که ادرار کودکشان پس از برخورد با هوا ، تیره رنگ میشد ( پوشاک نوزاد در بخش جلو قهوهای تیره تا سیاه میشد). سه سال بعد، کودک دیگری در همان خانواده به دنیا آمد که به همین بیماری دچار بود. مشاهد ههای آغازین گرود نشان داد، این بیماری در خانوادهها تکرار میشود، یعنی اگر یکی از خویشاوندان نسبی این صفت را داشته باشد، احتمال بروز آن در خویشاوندان دیگر نیز هست. اما به طور معمول، والدین کودکان بیمار ، این صفت را ندارند.
مسئله:
- چرا ادرار کودکان دچار شده به آلکاپتونوریا ، پس از برخورد با هوا، تیره میشود؟
- آیا این بیماری ارثی است؟
- الگوی توارث آن چگونه است؟
گردآوری اطلاعات:
در سال 1859، شیمیدانها ثابت کردند در ادرار این بیماران ترکیبی به نام اسید هموجنتیسیک (آلکا پت ون) وجود داردکه پس از واکنش با اکسیژن هوا ، به ماده ی سیاه رنگی تبدیل میشود و ساختمان شیمیایی آن، شبیه ملانین (رنگیز ه ی پوست) است.
چند پژوهشگر مقدار اسید هموجنتسیک ادرار بیماران را اندازهگیری کردند.
|
شماره |
جنسیت |
سن (سال) |
اسید هموجنتیسیک (گرم) |
پژوهشگر |
|
1 |
مرد |
5/2 |
2/3 |
اریک مایر |
|
2 |
مرد |
5/3 |
6/2 |
آرچیبلد گرود |
|
3 |
مرد |
8 |
7/2 |
ایوالد استایر |
|
4 |
مرد |
18 |
9/5 |
استانج |
|
5 |
مرد |
44 |
6/4 |
میتلباخ |
|
6 |
مرد |
45 |
7/4 |
اوگدن |
|
7 |
مرد |
60 |
3/5 |
هامارستن |
|
8 |
زن |
60 |
3/2 |
املسن |
|
9 |
مرد |
68 |
8/4 |
ولکاو/ بومن |
توجه: میانگین ترشح اسید هموجنتیسیک به گرم در 24 ساعت و با رژیم غذایی معمولی
پژوهشگران دریافتند :
1. این مولکول در ادرار افراد سالم وجود ندارد
2. همهی بیماران از کودکی این نارسایی را دارند
3. تغییر رژیم غذایی، باعث تغییر مقدار آلکاپتون در ادرار نمیشود
فرضیه سازی
دادههای جدول نشان میدهد، بین سن بیمار ا و میزان ترشح اسید هموجنتیسیک ( و در واقع ، بیماری آلکاپتونوریا ) ارتباطی وجود ندارد و مردها بیش از زنها به این بیماری مادرزادی دچار میشوند. همچنین ، گرود و پژوهشگران دیگر دریافتند، بین این بیماری و رژیم غذایی افراد، ارتباط معناداری وجود
ندارد. از این رو، میتوان نتیجه گرفت، این بیماری به اختلالی در واکنشهای شیمیایی بیماران مربوط میشود و مبتلایان این نارسایی را از والدین خود به ارث بردهاند.
فرضیه : اگر این نارسایی ارثی باشد، احتمال بروز آن در بستگان بیمار (برادرها و خواهرها) نیز وجود دارد.
بررسی فرضیه
گرود، برای بررسی این فرضیه، اطلاعات مربوط به موارد بیماری را که پژوهشگران دیگر گزارش کرده بودند، بررسی کرد
|
شماره |
تعداد افراد خانواده (برادر و خواهر) |
تعداد مبتلایان به آلکاپتونوریا |
تعداد افراد عادی خانواده |
پژوهشگر |
|
1 |
14 |
4 |
10 |
پاوه |
|
2 |
4 |
3 |
1 |
کایرس |
|
3 |
7 |
3 |
4 |
وینتر نیز |
|
4 |
2 |
1 |
1 |
استایر |
|
5 |
2 |
2 |
0 |
بومن |
|
6 |
1 |
1 |
0 |
مایر |
|
7 |
10 |
1 |
9 |
نوکیولی |
|
8 |
5 |
2 |
3 |
گرود |
|
9 |
3 |
2 |
1 |
گرود |
|
جمع |
48 |
19 |
29 |
|
پرسش1 : دادههای جدول را چگونه تفسیر میکنید؟ آیا این دادهها فرضی هی گرود را ثابت میکنند؟
الکاپتون از کجا میآید ؟
بررسیهای گرود نشان داد، آلکاپتونوریا یک بیماری ارثی است. اما چرا در ادرار مبتلایان مقدار زیادی آلکاپتون وجود دارد؟ در آن زمان، شیمیدانهایی که دربار هی واک نشهای زیست شیمیایی مطالعه میکردند، میدانستند که آنزیمها باعث سرعت این واکنشها میشوند و در نبود آنزیم، این واکنشها انجام نمیشوند. آنان نشان داده بودند که واکنشهایی زیست شیمیایی زنجیره و ا ر انجام میشوند؛ به طوری که ماد هی آغازین ، نخست به چند ماد هی میانی و سپس به فراورده تبدیل میشود. هر کدام از مرحل ههای یک زنجیر هی زیست شیمیایی را یک آنزیم پیش میبرد و اگر یکی از آنزیمها وجود نداشته باشند، ماد هی میانی، که آن آنزیم روی آن کار میکند، انباشته میشود و در صورتی که در آب محلول باشد، با ادرار به بیرون راه مییابد .
فرضیه سازی
ساختمان شیمیایی اسید هموجنتیسیک شباهت زیادی به ساختمان شیمیایی اسید آمین هی تیروزین دارد. (شکل زیر ). از این رو به نظر میرسد، اسید هموجنتیسیک از این اسید آمینه به دست میآید . افراد دچار شده به آلکاپتونوریا ، آنزیمی را که ماد هی میانی آلکاپتون را به مادهی میانی دیگری تبدیل میکند ، ندارند.
فرضیه: اگر این بیماری پیامد کمبود آنزیمی باشد که روی اسید هموجنتیسیک اثر میگذارد، پس میزان فعالیت این آنزیم باید در بیماران پایین باشد.
بررسی فرضیه
شکل زیر فعالیت آنزیم را در سه گروه افراد عادی، والدین بیماران و افراد بیمار نشان میدهد.
پرسش2 : با توجه به شکل، آیا فرضیه ثابت میشود؟ ادرار والدین بیماران ، پس از قرار گرفتن در معرض هوا به رنگ تیره در نمیآید. با وجود این، فعالیت آنزیم در آنان از افراد عادی کمتر است. این حقیقت را چگونه توجیه میکنید؟ اگر به هر سه گروه مقداری اسید هموجنتیسیک بخورانیم، انتظار دارید ترکیب ادرار آنان چه تغییری پیدا کند؟
50 سال طول کشید تا با نمونهبرداری از کبد مشخص شد، فعالیت آنزیمهای درگیر در تجزی هی اسیدآمینههای فنیل آلانین و تیروزین در افراد سالم و بیمار، به جز آنزیم هموجنتیسیک اسید اکسیداز، یکسان است (شکل زیر ). این آنزیم هموجنتیسیک را به مالیل استواستیک تبدیل میکند و کمبود فعالیت آن، باعث انباشته شدن این اسید در سلولها و سرانجام ترشح آن به ادرار میشود.
پرسش 3 : کودک دو سالهای به بیمارستان آورده شده است. مادرش میگوید، او زیاد استفراغ میکند ( به ویژه پس از شیر خوردن ). وزن کودک و میزان تحرکش زیر اندازهی عادی است. موهایش تیرهاند، اما رگههای سفیدی دارند. نتیج هی بررسی ادرار کودک به صورت زیر است.
|
غلظت برحسب میلی مول | ||
|
ماده |
ادرار بیمار |
ادرار عادی |
|
فنیل آلانین فنیل پیرووات فنیل استات |
0/7 8/4 3/10 |
01/0 0 0 |
الف) با توجه به شکل زیر ، این کودک دچار کمبود چه آنزیمی است؟
ب) برای درمان کودک، چه پیشنهادی دارید.
ج) چرا موهای کودک، رگههای سفید دارند؟
پژوهشهای فراکلاسی
1. همان طور که گفته شد، اسید هموجنتیسیک در برخورد با هوا به مادهای سیاه رنگ تبدیل میشود که ساختمان آن شبیه ملانین (رنگیز هی پوست) است. پژوهش کنید، بین سوخت و ساز ملانین و اسیدهموجنتیسیک چه ارتباطی وجود دارد؟
2. آلبینیسم یکی دیگر از نارسایی مادر زادی در سوخت و ساز است. این نارسایی که به کاهش تولید ملانین و در نتیجه سفید شدن مو میانجامد، به علت کمبود فعالیت یکی از آنزیمهای دخیل در تولید ملانین به وجود میآید. دربار هی این نارسایی اطلاعات بیشتری گردآوری کنید.
3. فنیل کتونوریا ( PKA ) نوعی نارسایی مادرزادی در سوخت و ساز است که بر خلاف دو نارسایی دیگر که گفته شد، میتواند با پیامدهای خطرناکی مانند کند ذهنی همراه باشد. دربار هی این نارسایی و چگونگی کا ستن از پیامدهای آن پژوهش کنید.
منبع:
Archibald E.Garrod, The Incidence of Alkaptonuria A: Study in Chemical Individuality, Lancet, Vol. Ii, 1902, pp.1616-1620
بیماری هانتینگتون
بیماری هانتینگتون
شرح حال بالینی
M.P مرد 45 سالهای است که در ابتدا با کاهش حافظه و قدرت تمرکز مراجعه کرد. با زوال عملکرد هوشی در طی سالهای بعد ، او دچار حرکات غیر ارادی انگشتان دست و پا و نیز حرکات کج و معوج صورت و لبها شد. او از وضعیت خودآگاه و افسرده بود. او قبلا سالم بود و سابقه ابتلای مشابهی در بستگان خود نداشت. والدینش در دهه پنجم عمر خود در یک سانحه رانندگی جان سپرده بودند. M.P یک دختر سالم داشت. پس از ارزیابی وسیع ، متخصص و داخلی اعصاب ، وضعیت M.P را بیماری هانتیگتون تشخیص داد.علت بیماری
هانتینگتون ، نوعی اختلال تحلیل برنده عصبی اتوزومی غالب است که در تمام نژادها به چشم میخورد و به علت جهشهایی در ژن HD ایجاد میشود.بیماریزایی
فرآورده ژن HD ، یعنی هانتینگتون در همه جا بروز مییابد. عملکرد این ژن ناشناخته مانده است. جهشهای بیماریزا در HD ، معمولا ناشی از بسط یک توالی تکراری CAG رمزگردانی کننده پلیگلوتامین در اگزون 1 میباشند. اللهای طبیعی HD ، حدود 10 تا 26 تکرار CAG دارند، در حالی که اللهای جهش یافته واجد بیش از 36 تکرار میباشند.تقریبا 3 درصد بیماران در نتیجه بسط تکراری CAG جدید دچار هانتینگتون میشوند، در حالی که 97 درصد الل HD جهش یافتهای را از یک والد مبتلا به ارث میبرند. بروز هانتینگتین جهش یافته موجب اختلال عملکرد نورونی ، آتروفی فراگیر مغز ، تغییرات در سطوح گیرندههای عصبی و تجمعات هستهای و سیتوپلاسمی نورونها میشود، سرانجام باعث مرگ نورونی میگردد.
فنوتیپ و سیر طبیعی
سن بیمار در شروع بیماری ، نسبت عکس با تعداد تکرارهای CAG در HD دارد ، افرادی که بیماری آنها در بزرگسالی تظاهر کرده است، معمولا 40 تا 55 تکرار دارند، در حالی که افراد دچار بیماری با تظاهر در نوجوانی بیش از 60 تکرار دارند. از آنجا که طول تکرار CAG رابطه عکس با سن تظاهر دارند، افرادی که جهش از پدرشان به ارث بردهاند، در معرض خطر افزایش یافته ابتلا به بیماری با تظاهر زودرس میباشند.تقریبا 80 درصد بیماران نوجوان ، ژن HD جهش یافته را از پدر به ارث میبرند. تقریبا 3/1 بیماران با اختلالات روانی تظاهر میکنند. 3/2 با ترکیبی از اختلالات شناختی و حرکتی مراجعه میکنند. هانتینگتون با اختلالات پیشرونده حرکتی ، شناختی و روانی مشخص میشود. اختلالات حرکتی شامل حرکات ارادی و نیز غیرارادی میشوند. در ابتدا این حرکات به میزان ناچیزی در فعالیتهای روزانه مداخله میکنند، اما با پیشرفت بیماری ، عموما ناتوانکننده میشوند.
کره که در بیش از 90 درصد بیماران وجود دارد، شایعترین حرکت غیرارادی است. کره با پرشهای غیرتکراری و غیردورهای که بطور ارادی قابل سرکوب کردن نیستند، مشخص میشود. اختلالات شناختی ، در اوایل سیر بیماری آغاز میگردد و بر تمام جنبههای شناخت تاثیر میگذارد. زبان معمولا دیرتر از سایر اعمال شناختی درگیر میشود.
اختلالات رفتاری که معمولا در مراحل دیررستر سیر بیماری بروز میکنند عبارتند از: مهار گسیختگی اجتماعی ، خلق تهاجمی ، خشم ناگهانی ، بیتفاوتی ، انحراف جنسی و افزایش اشتها. تظاهرات روانی که میتواند در هر زمانی از سیر بیماری ایجاد شوند، شامل تغییرات شخصیتی و اسکیزوفرنی میباشند.
اداره بیماری
در حال حاضر ، هیچ درمان علاج دهندهای برای بیماری هانتینگتون وجود ندارد. درمان بر مراقبت حمایتی و نیز اداره دارویی مشکلات رفتاری و عصبی متمرکز است.خطر توارث
هر یک از فرزندان فردی مبتلا به هانتینگتون ، به احتمال 50 درصد نوعی الل HD جهش یافته را به ارث میبرد. بجز اللهای دارای نفوذ ناکامل ، تمام فرزندان به ارث برنده الل جهش یافته HD ، در صورتی که عمر طبیعی داشته باشند، دچار هانتینگتون خواهند شد.
بر گرفته از مجله رشد